Апластическая анемия
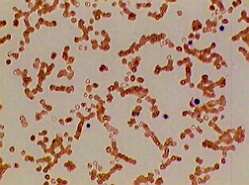 Апластическая анемия – это наследная либо обретенная патология крови, обусловленная поражением стволовых клеток костного мозга, вследствие которого развивается глубочайшее подавление гемопоэза. 1-ые сведения о апластической анемии были получены еще в 1888 году, но насколько самостоятельная нозологическая единица апластическая анемия была зарегистрирована исключительно в 1904 году.
Апластическая анемия – это наследная либо обретенная патология крови, обусловленная поражением стволовых клеток костного мозга, вследствие которого развивается глубочайшее подавление гемопоэза. 1-ые сведения о апластической анемии были получены еще в 1888 году, но насколько самостоятельная нозологическая единица апластическая анемия была зарегистрирована исключительно в 1904 году.
Гипопластическая анемия относится к самой тяжеленной форме нарушения кроветворения, потому что летальность при апластической анемии добивается порога 80%.
Не следует путать апластичесую анемию, которая является отдельной нозологической формой с гипопластическим синдромом, который является только одним из бессчетных проявлений разных болезней, сопровождающихся нарушением функции кроветворения костного мозга.
К счастью, частота встречаемости случаев апластической анемии не превосходит 5 эпизодов на 1000000 населения, но опасность данной патологии состоит в том, что она поражает в главном лиц детского и юного возраста. Половая принадлежность не имеет воздействия на течение и финал заболевания.
Апластическая анемия причины
Данная патология относится к категории полиэтиологичных болезней, другими словами существует огромное количество обстоятельств, одна из которых может занять доминирующую позицию и спровоцировать нарушение в системе кроветворения у того либо другого хворого. Не считая того, различают так именуемые причины риска, другими словами предрасполагающие причины, совокупа которых может не только лишь поспособствовать развитию заболевания, да и ухудшить течение патологического процесса. К счастью, почти всегда удается распознать этиологический фактор, который стал первопричиной развития признаков анемии, но встречаются ситуации, когда найти этиопатогенетический фактор не удается и в таком случае устанавливается диагноз «идиопатическая апластическая анемия».
Часто апластическая анемия выступает в роли побочной реакции от внедрения определенных групп фармацевтических средств, при этом появление ее не зависит ни от дозы, ни от длительности приема данного продукта. К фармацевтическим средствам, способным стимулировать нарушения всех ростков кроветворения в костном мозге относятся: антигистамины, сульфаниламиды, лекарства тетрациклинового ряда, также препараты золота. В особенности нередко апластическая анемия встречается у лиц, принимающих Левомецитин.
Отдельно следует упомянуть роль ионизирующего излучения, применяющегося в рентгенологических способах исследования, в появлении признаков апластической анемии. Данная патология встречается посреди лиц, работающих в рентгенологических кабинетах и у пациентов, подвергающихся радиоволновой терапии.
Кроме того, провокаторами апластической анемии могут стать заболевания вирусной этиологии в остром периоде (вирусный гепатит, цитомегаловирусная и герпетическая зараза, ВИЧ).
Среди гематологов существует мировоззрение, что во время беременности увеличивается риск появления апластических нарушений в костном мозге, но патогенетического разъяснения этому процессу пока не найдено. Необходимо подчеркнуть, что выявление признаков апластической анемии является абсолютным показанием для прерывания беременности, и зарегистрированы случаи перехода заболевания в стадию ремиссии после искусственного родоразрешения.
Еще одной предпосылкой появления апластической анемии является токсическое воздействие на организм препаратов, применяющихся в качестве химиотерапии для исцеления онкопатологии, также долгое пребывание в критериях воздействия паров пестицидов и инсектицидов.
Среди обстоятельств нарушения кроветворной функции костного мозга следует рассматривать и аутоиммунные заболевания, при которых иммунные механизмы ориентированы на ликвидирование не только лишь болезнетворных агентов, да и на повреждение собственных клеток костной ткани.
Апластическая анемия симптомы
Для апластической анемии типично медлительно-прогрессирующее течение со склонностью к переходу в приобретенную форму с периодами обострений.
Все клинические симптомы, наблюдающиеся при апластической анемии можно отнести к одному из 3-х главных синдромов: анемичного, геморрагического либо симптомокоплекса заразных осложнений. Возникновение признаков того либо другого синдрома является следствием подавления 1-го либо нескольких ростков кроветворения.
Основными жалобами пациентов при развитии презнаков анемичного синдрома, обусловленного недостающим уровнем гемоглобина и эритроцитов в периферической крови, являются: выраженная слабость и понижение трудоспособности, головокружение и шум в ушах при сохранности слуха, чувство нехватки воздуха и приступы учащения сердцебиения.
Первыми признаками появления геморрагического синдрома у пациента с апластической анемией является возникновение кровоподтеков и гематом на кожных покровах нетравматического происхождения. Пациенты с апластической анемией нередко сетуют на носовые кровотечения, также кровоточивость десен. При выраженном угнетении тромбоцитарного ростка кроветворения может появиться кровоизлияние в мозг.
Симптомами понижения уровня лейкоцитов, насколько 1-го из патогенетических звеньев апластической анемии, является расположенность к болезням заразной природы. Такие нездоровые относятся к категории «нередко болеющие», другими словами в течение года у их наблюдается более 10 эпизодов заразных болезней. Выраженное подавление выработки лейкоцитов провоцирует гнойно-септические отягощения (язвенно-некротическая ангина, афтозный стоматит, отит, панариций, постинфекционные абсцессы, генерализованный сепсис).
Уже при первичном осмотре пациента можно найти соответствующие симптомы апластической анемии: выраженная бледнота и синюшность кожных покровов с наличием кровоподтеков, не имеющих точных границ, а время от времени и мелкоточечной петехиальной сыпи. Повышение границ печени и возникновение отеков нижних конечностей свидетельствуют о развитии признаков сердечной дефицитности. Аускультативно отмечается склонность к гипотензии, синусовая тахикардия и твердый систолический шум во всех аускультативных точках. Принципиальным диагностическим признаком апластической анемии является неизмененная в размерах селезенка.
Степень проявления того либо другого симптомокомплекса впрямую находится в зависимости от степени подавления ростков кроветворения. Апластическая анемия тяжеленной формы имеет такие диагностические аспекты: уровень нейтрофилов наименее 0,5?109/л, тромбоциты наименее 20?109/л, корригированное повышение ретикулоцитов наименее 1%. Если у хворого имеется хотя бы один из этих критериев в купе с выраженным понижением клеточности костного мозга, то это является поводом для установления пациенту диагноза «гипопластическая анемия тяжеленной степени».
Апластическая анемия у детей
В детском возрасте почаще дебютируют прирожденные типы апластических анемий, к которым относятся анемии Фанкони и Блекфена-Даймонда.
Анемия Фанкони представляет собой наследную патологию, наследуемую по аутосомно-рецессивному типу, другими словами случаи заболевания наблюдаются исключительно в семьях, где оба родителя являются носителями патологического гена. Проявляется анемия Фанкони не только лишь в глубочайшем угнетении всех типов кроветворения, да и в возникновении аномалий развития.
Дебют заболевания приходится на возраст 4-12 лет, но гематологические задачи могут появиться конкретно после рождения ребеночка. К прирожденным аномалиям относятся: несоответствие костного возраста паспортному, прирожденные пороки сердечно-сосудистой системы, микроцефалия, аномалии развития костной ткани, органов мочеполовой системы, отставание в психомоторном развитии. Гематологические конфигурации появляются в более позднем возрасте (в среднем по достижению 9 лет) и в медицинской картине преобладают симптомы геморрагического симптомокомплекса, после этого прогрессивно нарастают признаки лейкоцитопении и эритроцитопении.
Данная патология имеет быстрое прогрессирующее течение, потому при отсутствии адекватного исцеления смертельный финал наступает в течение 6 месяцев. Предпосылкой погибели в большинстве случаев является мощное желудочно-кишечное кровотечение либо мозговое кровоизлияние. Отягощениями анемии Фанкони является трансформация заболевания в острый лейкоз, также онкопатология органов желудочно-кишечника. Единственным действенным способом исцеления прирожденной анемии Фанкони является трансплантация костного мозга.
Анемия Блекфена-Даймонда относится к группе спорадических наследных патологий крови и характеризуется поражением только эритроцитарного ростка кроветворения. Дебют заболевания наблюдается в течение первого года жизни ребеночка.
Дети с анемией Блекфена-Даймонда имеют обычный фенотип: бледноватые кожные покровы, большая верхняя губа, обширно поставленные глаза, сухие секущиеся волосы, отставание костного возраста от паспортного.
Характерным конфигурацией лабораторных характеристик периферической крови является прогрессирующая нормохромная анемия при полной сохранности пролиферации клеток тромбоцитарного и гранулоцитарного ряда.
Данная патология характеризуется вялотекущим приобретенным течением со склонностью к спонтанной ремиссии. Желаемым способом исцеления является пременение кортикостероидной терапии, также по актуальным свидетельствам переливание эритроцитарной массы.
В детском возрасте обретенные формы апластической анемии встречаются очень изредка и появляются теми же симптомами, что и у взрослых при полном отсутствии прирожденных патологий.
При наличии у ребеночка признаков нарушения кроветворной функции костного мозга непременно нужно проводить дифференциальную диагностику с такими болезнями насколько: острый лимфобластный и миелобластный лейкоз, мегалобластная анемия, синдром гиперспленизма, метастатическое поражение костного мозга.
Ребенок с подозрением на прирожденную апластическую анемию непременно подлежит всеохватывающему обследованию, к которому относятся: цитогенетический анализ после трепанобиопсии, анализ крови на предмет наличия антител к клеточкам крови, рентгенография с определением костного возраста, миелограмма. Также обследованию подлежат все наиблежайшие родственники хворого ребеночка.
Апластическая анемия лечение
Залогом скорого излечения пациентов с апластической анемией является ранешняя диагностика данного патологического состояния, адекватная оценка тяжести состояния пациента, также личный подход к выбору целесообразного в каждом определенном случае способа исцеления.
Впервые диагностированная апластическая анемия является поводам для госпитализации хворого в стационар, независимо от выраженности клинических проявлений и лабораторных характеристик.
В ситуации, когда известен этиопатогенетический фактор, спровоцировавший развитие апластической анемии, исцеление нужно начинать с устранения первопричины, во избежание предстоящего прогрессирования подавления процессов кроветворения.
В качестве целительных мероприятий пре диагностированной апластической анемии гематологи в мире используют последующие методики: заменное переливание цельной крови либо ее частей, трансплантация костного мозга, также применение фармацевтических средств, направленных на стимуляцию процессов кроветворения.
Заместительная терапия апластической анемии предполагает внедрение заменного переливания подходящей донорской крови либо отдельных ее частей (тромбоцитарная, эритроцитарная масса и гранулоциты). Данный способ исцеления является превентивным, потому что переливание крови только восполняет припас нужных частей крови, но не восстанавливает функцию кроветворения в костном мозге. Не считая того, при таковой форме апластической анемии, насколько аутоиммунная, данный способ не применяется, потому что на введение чужеродных клеток организм начинает производить иммунный ответ, что обусловливает неэффективность исцеления.
Следует учесть, что неоднократные вливания донорской крови сопровождаются лишним скоплением железа в организме, которое откладывается в актуально-принципиальных органах, нарушая их структуру. В данном случае целенаправлено соединять переливание крови с приемом препаратов, содействующих выведению железа из организма. Во избежание процесса отторжения трансплантата перед процедурой пересадки костного мозга нездоровому нецелесообразно использовать переливание компонент крови.
Самым действенным и в то же время самым небезопасным способом исцеления апластической анемии является трансплантация костного мозга, так как этот способ может стать пусковым механизмом для нормализации функции кроветворения костного мозга. Данный способ употребляется желательно в юном возрасте пациента после кропотливого подбора подходящего донора, коим может стать ближний родственник пациента. Предварительными процедурами при трансплантации стволовых клеток костного мозга являются воздействие на организм хворого больших доз радиоактивного облучения, также применение препаратов химиотерапии. Предварительным шагом со стороны донора является забор крови, фильтрация из нее здоровых стволовых клеток и введение их в общий кровоток пациента, при помощи которого они попадают в костномозговые полости, где и происходит пролиферация здоровых кровяных клеток.
Во избежание осложнений, нездоровому назначаются препараты, предотвращающие отторжение трансплантата, но не всегда удается избежать этой фатальной для пациента ситуации. Данный способ исцеления является дорогостоящим и просит соблюдения определенных критерий, которые доступны исключительно в специализированных клиниках, в связи с чем же не получает широкого использования в качестве терапии апластической анемии.
Больные с апластической анемией аутоиммунного генеза нуждаются в применении иммуносупрессивных препаратов, действие которых ориентировано на угнетение неадекватного функционирования иммунной системы. Продуктами выбора в данной ситуации числятся: Циклоспорин (дневная доза составляет 10 мг/кг перорально), Антитимоцитарный глобулин (дневная доза 15 мг/кг внутривенно) и Антилимфоцитарный глобулин (дневная доза 130 мг внутривенно капельно). Применение иммунодепрессантов почти всегда сопровождается выраженными побочными реакциями, угрожающими жизни пациента (анафилактический шок, сывороточная болезнь, заразные заболевания), для предотвращения которых целенаправлено использовать кортикостероидные препараты (Преднизолон в дневной дозе 1 мг/кг). Безусловно, иммуносупрессивная терапия является одним из самых действенных способов исцеления апластической анемии, но встречаются случаи, когда после приема препаратов этой группы наблюдается рецидив заболевания.
В качестве дополнительной терапии к основному направлению в лечении апластической анемии используются препараты, стимулирующие кроветворную функцию костного мозга, так именуемые колониестимулирующие причины (Молграмостин, Филграстим, Лейкомакс). Препараты этой группы эффективны в отношении стимуляции пролиферации клеток гранулоцитарного ряда, потому областью их внедрения являются случаи апластической анемии, сопровождающиеся выраженной лейкоцитопенией. Курс терапии колониестимулирующими факторами составляет более 2-ух недель и желаемым способом введения препаратов является парентеральный в дневной дозе 5 мг/кг. Ограничивающим фактором в применении средств этой группы является их высочайшая цена.
Научно подтверждено стимулирующее действие андрогенов на все ростки кроветворения, в связи с чем, в текущее время обширно пременяется терапия андрогенами в лечении апластической анемии. Данные препараты целенаправлено использовать исключительно в случае заболеваемости посреди парней, и рекомендованы долгие курсы введения препаратов (Тестостерона пропионат два раза в день по 1 мл 5% раствора либо пролонгированный продукт Сустанон - 250 1 мл 1 раз за месяц).
В качестве паллиативного способа исцеления употребляется конструктивная спленэктомия, которая в 85% случаев имеет полезный эффект в лечении апластической анемии. Патогенетической обоснованностью данного способа будет то, что при удалении селезенки прекращается секвестрация кровяных клеток и резко ограничивается продукция антител против собственных здоровых клеток костного мозга. Данный способ исцеления показан всем нездоровым без признаков заразных осложнений.
Апластическая анемия прогноз
Прогноз для жизни, трудоспособности и состояния здоровья пациентов с признаками апластической анемии впрямую находится в зависимости от степени тяжести заболевания и глубины понижения уровня актуально принципиальных клеток кроветворения.
К огорчению, до настоящего времени, глобальная статистика указывает неутешительные данные в отношении показателя смертности от апластической анемии, независимо от того, как прогрессивно развивается лекарственная ветвь в отношении исцеления заболеваний крови. Высочайшая смертность наблюдается посреди пациентов с тяжеленной формой панцитопении и в основном предпосылкой погибели является генерализованная форма сепсиса, насколько конечная стадия лейкоцитопении.
Значительно стали лучше прогнозы после начала внедрения конструктивных способов исцеления (трансплантация стволовых клеток костного мозга, внедрение иммунодепрессантов). В 50-90% случаев применение этих методов исцеления можно достигнуть полного излечения пациента.
Применение Антитимоцитарного и Антилимфоцитарного иммуноглобулинов в купе с терапией Циклоспорином позволяют только в 60-70% случаев достигнуть ремиссии заболевания.
26.04.2024